Batteries lithium-air : des chercheurs américains innovent et fondent l’espoir d’une percée technologique
La suite de votre contenu après cette annonce

Une découverte récente des chercheurs de l’Université de Chicago et de l’Argonne National Laboratory pourrait amener les industriels à reconsidérer la batterie lithium-air comme technologie d’avenir pour les véhicules électriques
Aux quatre coins de la planète, des scientifiques et des industriels s’affairent à mettre au point de nouvelles technologies de batterie. Objectif : remédier aux limites actuelles des accumulateurs lithium-ion qui équipent la plupart de nos smartphones, ordinateurs portables, voitures électriques ainsi que de multiples autres appareils « nomades ».
Prix, poids, volume, vitesse de charge et capacité de stockage : voilà les caractéristiques des batteries que les laboratoires du monde entier tentent d‘améliorer. Avec en prime le souci d’utiliser des matériaux dont les réserves mondiales sont moins critiques et problématiques que celles du cobalt par exemple.
Dans les cartons des chercheurs on trouve notamment la technologie lithium-air ( ou lithium-oxygène : Li-O2 ) qui a suscité quelques espoirs au cours des dernières années. C’est que, sur le papier, ses propriétés ont de quoi convaincre : à poids égal une batterie lithium-air serait capable de stocker jusqu’à 5 fois plus d’électricité que les accumulateurs lithium-ion. Pour fonctionner elle n’utilise, outre le lithium et l’air, que du carbone, un des éléments les plus répandus dans la croûte terrestre et extrêmement bon marché. Mais surtout, l’oxygène utilisé comme matière première pour alimenter la réaction chimique avec le lithium pendant la décharge de la batterie, peut être puisé gratuitement, partout et sans limite dans l’air ambiant. Nul besoin, en théorie donc, de le stocker et le transporter dans le véhicule. On imagine aisément le gain en termes de coût, de poids et de volume.
Malheureusement les efforts pour mettre au point la technologie lithium-air se sont heurtés à des problèmes pratiques qui ont entravé son développement.
Pendant la décharge de la batterie, c’est-à-dire pendant l’utilisation de la voiture ou de l’appareil, la réaction du lithium avec l’oxygène engendre, dans la cathode, du peroxyde de lithium (Li2O2). Lorsque l’accumulateur se recharge, ce composé se dissocie : les ions lithium repartent vers l’anode et l’oxygène est libéré dans l’air sous forme gazeuse. C’est un peu comme si ces batteries inspiraient puis expiraient de l’oxygène.
Un peroxyde de lithium qui pose des soucis. Lorsqu’il s’accumule sur la cathode constituée de carbone poreux, il finit par l’encrasser, bouchant tous les interstices et bloquant ainsi les réactions chimiques ultérieures. En outre ce Li2O2 est un composé chimique très réactif et agressif. Il provoque notamment une oxydation de l’anode en lithium. Des réactions « parasites » se forment également avec d’autres composés contenus dans l’air, notamment le dioxyde de carbone et la vapeur d’eau. Des sous-produits indésirables se déposent sur la cathode qui finit par être complètement enrobée et incapable de fonctionner. Après seulement quelques cycles de charge-décharge, les performances de la batterie s’effondrent. Pour y remédier, des chercheurs ont tenté d’utiliser, au lieu de l’air ambiant, de l’oxygène pur contenu dans des bouteilles. Mais cette pratique annule les avantages de la technologie tout en posant de sérieux problèmes de sécurité dus au risque d’incendie que peut provoquer l’oxygène pur.
D’autres laboratoires ont essayé de contourner les difficultés par d‘autres astuces mais jusqu’à présent ils n’avaient pas réussi à mettre au point une batterie lithium-air dotée d’une durée de vie acceptable.
Nouvelle architecture
Une équipe constituée de scientifiques de l’Université de l’Illinois à Chicago (UIC) et du Laboratoire National de l’Argonne a réussi à surmonter ces obstacles. Les résultats de leurs travaux ont fait l’objet d’une publication dans la fameuse revue scientifique Nature ce 21 mars 2018.
Ils ont enduit l’anode d’une fine couche de carbonate de lithium qui permet aux ions lithium de passer au travers pour migrer vers l’électrolyte, mais empêche l’oxydation de l’anode. Pour protéger la cathode qui est l’endroit par où l’air entre dans la batterie au travers d’une structure en treillis poreux à base de carbone, les scientifiques américains l’ont recouverte de bisulfure de molybdène qui joue le rôle d’un catalyseur. Quant à la composition de l’électrolyte à base de diméthylsulfoxyde, un solvant polaire organique utilisé communément dans les batteries, il permet de faciliter les réactions lithium-oxygène, minimise les réactions indésirables du lithium avec les autres constituants de l’air et augmente l’efficacité de la batterie. Cette conception permet d‘utiliser l’air ambiant et de maintenir les performances de l’accumulateur pendant plus de 750 cycles complets de charge et décharge, ce qui est exceptionnel.
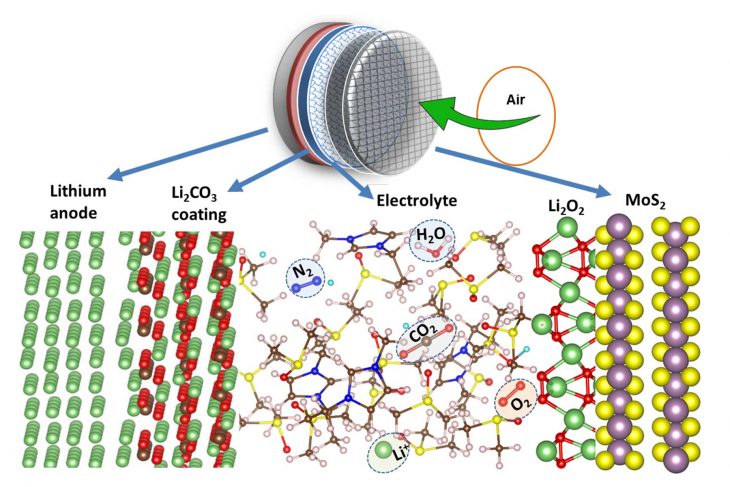
« Nous avons réaménagé et redessiné complètement l’architecture de cette batterie ce qui nous a permis d’activer les réactions chimiques que nous voulions voir se produire et d’empêcher ou bloquer celles qui finissent par entraîner la mort de la batterie« , a déclaré Salehi-Khojin, l’un des membres de l’équipe de chercheurs.
Bien qu’un pas important semble ainsi avoir été fait vers l’industrialisation et la commercialisation des batteries lithium-air, de nombreuses autres étapes doivent encore être accomplies avant de les voir équiper nos voitures et appareils nomades.
Source : Communiqué de l’UIC
La suite de votre contenu après cette annonce
sur l'actualité électrique
Le meilleur d'Automobile Propre, dans votre boite mail !
Découvrez nos thématiques voiture électrique, voiture hybride, équipements & services et bien d’autres
S'inscrire gratuitement







